10月16日,Cell research在线宣布了中国科学院分子植物科学杰出立异中心张鹏研讨组题为Crystal structure of plant PLDα1 reveals catalytic and regulatory mechanisms of eukaryotic phospholipase D的研讨论文。该研讨解析了植物磷脂酶Dα1及其与产品磷脂酸(PA)复合体的晶体结构,具体阐释了真核生物磷脂酶D催化磷脂发作磷脂酸及其活性调理的分子机制。
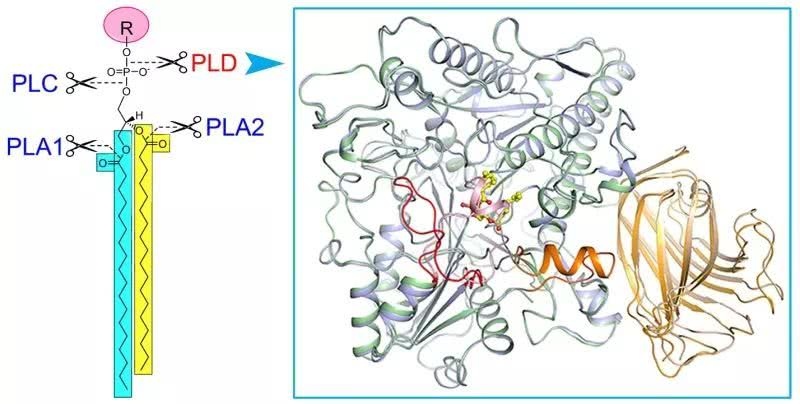
磷脂酶(Phospholipase, PL)催化细胞膜上磷脂的水解。依据水解部分的不同,人们将磷脂酶分红磷脂酶A1、A2、C和磷脂酶D (PLD)(图1)。磷脂酶的功用一方面经过酰基搬运完成细胞内磷脂的从头组成与分配;另一方面水解发作脂质信号分子,调控生物体许多重要生理进程,如PLC水解PIP2发作三磷酸肌醇(IP3)和二酰基甘油(DG),PLD水解多种磷脂发作PA。真核生物PLD最先在植物中克隆判定,之后在动物及其他生物体中连续得到判定,是生物中高度保存的一类酶。在结构域组成上,PLD包含N端结合磷脂/细胞膜的PX/PH/C2结构域和C端担任催化的HKD结构域。研讨发现动物PLD1/2与细胞的生长发育、癌症发作、神经系统疾病如阿尔兹海默症、病毒侵略等疾病的发作亲近相关。在植物中,有多达十几种PLD(α1-3、β1-2、γ1-3、δ、ε、ζ1-2)被连续判定。其间ζ1-2与动物中的PLD1/2类似,均归于PX/PH型PLD,其他归于植物特有C2型PLD。植物PLD在体内参加了多种重要生理与病理进程,包含:低温/干旱相应、病原侵染、种子萌生、花粉管伸长、根的发育等。但是,比较于其他三类磷脂酶(A1/A2/C),人们对PLD蛋白的三维结构、催化以及活性调控机制缺少了解。
在该研讨中,研讨人员以高等植物PLD蛋白作为研讨方针,成功表达与纯化了有活性的方针蛋白,从而解析了拟南芥PLDα1处于底物非结合态及与产品PA结合态的晶体结构(图1)。这是初次取得真核生物磷脂酶D的三维结构。结构剖析提醒了:1)底物的结合口袋是处于两个HKD结构域之间的一个很大的疏水空腔,口袋上方有一个α螺旋和loop组成的盖子,在底物非结合态时,盖子掩盖在口袋上方,处于封闭状况;在产品PA(或底物)结合时,盖子发作构象变化呈敞开状况,答应底物进入或许产品结合与开释。2)担任催化底物催化的两个HKD motif呈空间排布且保存,更正了曾经文献报导中的过错。3)在活性中心邻近存在一个保存的钙离子结合位点,为C2型PLD发挥活性所有必要。这一位点在PX/PH型PLD中不存在,很好地解说了为什么C2型PLD需求钙离子激活,而PX/PH型PLD发挥活性不需求钙离子。4)C2结构域与催化结构域的互作网络,C2结构域经过结合质膜/磷脂,从而将PLD定位到细胞膜,一起调理其催化活性。此外,该研讨还发现已知的动物PLD1/2小分子按捺剂能够按捺PLDα1的活性,标明真核生物PLD蛋白具有类似的结构和催化/按捺机制。这些研讨结果使人们对真核生物PLD蛋白的催化和活性调理机制有了全新的知道。研讨结果为以真核PLD蛋白为靶标的小分子按捺剂挑选及优化规划指明晰方向。
张鹏研讨组副研讨员李建戌和上海师范大学生命科学学院副研讨员俞芳是该论文的一起榜首作者,张鹏为该论文的通讯作者。该研讨得到中科院(先导B、青促会)、科技部、基金委及上海市的项目赞助。试验数据搜集作业得到上海光源19U1/17U1线站的支撑与协助。
图:脂酶D及晶体结构。左图显现不同磷脂酶(PLA1、PLA2、PLC、PLD)催化磷脂水解的位点,右图为磷脂酶D与产品磷脂酸(黄色棍棒模型)结合前后的三维结构叠加图,显现底物结合前后的构象变化。
来历:中国科学院分子植物科学杰出立异中心